A l’échelle de la plante la feuille est l’organe photosynthétique, à l’échelle du tissus c’est la cellule chlorophyllienne qui remplit ce rôle, et à l’intérieur de la cellule, l’organite spécialisé est une petite bille verte, chlorophyllienne appelée le chloroplaste. Seulement au delà de ces acteurs, comment mettre en évidence le bilan de la photosynthèse ? Quelles structures sont responsables de capturer l’énergie lumineuse ?
I- Mise en évidence de l’équation bilan
1) Matière Organique
Protocole :
a) réalisé uniquement par l’enseignant :
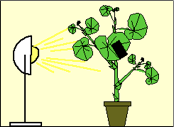 1. une feuille d’un Pélargonium est prélevée dont la feuille a porté un cache pendant 48h (feuilles panachées ou normale)ainsi qu’une autre feuille qui a été enveloppée dans un sachet de potasse et une feuille panachée.
1. une feuille d’un Pélargonium est prélevée dont la feuille a porté un cache pendant 48h (feuilles panachées ou normale)ainsi qu’une autre feuille qui a été enveloppée dans un sachet de potasse et une feuille panachée.
2. Ces feuilles sont mises dans une casserole remplie d’éthanol à 50% afin d’être décolorées totalement à l’ébulition.
(Explication : Les pigments photosynthétiques sont solubles dans des solvants organiques et peuvent donc être séparés à l’aide de solvants comme l’éthanol. Intérêt : Les pigments ainsi éliminés ne masqueront pas une éventuelle réaction avec l’eau iodée).
3. l’éthanol est vidé.
b) Protocole à poursuivre
4. Récupérer avec précaution les feuille décolorée et les déposer dans une boite de pétri.
5. Recouvrir d’eau iodée
7. Observer le résultat – Comparer les zones colorées par l’eau iodée et la répartition des zones pigmentées de la feuille pour les panachés et confronter avec les feuilles ayant été confinées avec la potasse.
Comment expliquer les différences de coloration des feuilles à l’eau iodée ?
Remarque : La potasse est une base forte et le CO2 est un acide faible. On a donc une réaction qui donne du carbonate de potassium, privant totalement le CO2 de l’atmosphère ambiant
2) Mise en évidence du rejet gazeux de la plante
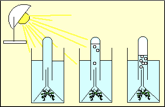 Seuls 4 cristallisoirs ont été mis en route
Seuls 4 cristallisoirs ont été mis en route
1- de l’Elodée ou du Cabomba ont été placées à la lumière afin de réaliser la photosynthèse.
2- Un entonnoir a été placé sur la plante surmonté d’un tube à essai afin de recueillir les gaz émis par la photosynthèse
3- Vous disposez de rouge crésol, afin d’observer le contenu en gaz (ou d’une allumette)
4- Plongez votre main dans le cristallisoir afin de boucher dans l’eau le tube a essai
5- rajoutez un peu de rouge crésol à votre contenu en gaz et agitez (ou utiliser l’allumette)
6- si le rouge crésol devient jaune => CO2 s’il devient violet => O2 (si l’alumette incandescente s’étouffe => CO2 ; Si au contraire elle se rallume => O2)
Quel est le bilan de ce qui est absorbé et de ce qui est rejeté par la plante chlorophyllienne à la lumière ?
3) Equation de la photosynthèse
Donner l’équation de la photosynthèse en justifiant les molécules d’après les expériences
II- Capter l’énergie lumineuse
Extraction des pigments photosynthétiques
Les feuilles vertes (comme les feuilles d’autres couleurs) contiennent un ensemble de pigments qui peuvent être séparés par chromatographie.
Ces pigments (contenus dans les chloroplastes et plus exactement dans les thylakoïdes) absorbent l’énergie lumineuse afin de réaliser la première phase de la photosynthèse (cette première phase est appelée phase photochimique).
On cherche donc à vérifier le fait que ces feuilles vertes possèdent bien différents pigments et qu’il permettent une interaction avec l’énergie lumineuse.
PRINCIPE DE LA CHROMATOGRAPHIE
C’est une technique de séparation des substances présentes dans un mélange ; elle utilise la migration d’un liquide (solvant) sur un support solide (papier..). Les constituants du mélange sont entraînés plus ou moins loin suivant leurs propriétés physico-chimiques (masse, polarité, solubilité…). Les pigments solubles dans le solvant migrent sur le papier de chromatographie et se répartissent de la façon suivante :

PROTOCOLE DE LA CHROMATOGRAPHIE
1. Préparer les éprouvettes : en veillant à prendre le papier uniquement par les bords pour éviter de poser les doigts sur la zone de migration, suspendre le papier à chromatographie à l’aide d’un crochet fixé sur un bouchon, le placer dans l’éprouvette pour repérer le niveau du solvant à mettre (le papier devra tremper d’un demi-cm dans le solvant).
2. Retirer le papier, verser précautionneusement le solvant (en évitant tout contact avec la peau et les yeux) jusqu’au niveau repéré et fermer les éprouvettes sans le papier.
3. Tracer un trait au crayon à 2 cm du bas de la bande de papier pour marquer l’emplacement du dépôt.
4. SOIT a) La tache de pigments doit être aussi petite et foncée que possible. Pour cela : écraser, à l’aide d’un agitateur et de la pince fine, un petit morceau de feuille à l’emplacement prévu sur la bande, répéter l’opération 3 fois, sur le même emplacement, en renouvelant le morceau de feuille.
OU b) extraire des pigments chlorophyllien selon les conseils de l’enseignant, et y appliquer 10 gouttes sur le dépôt (chaque goutte séchée par un sèche cheveux).
5. Suspendre le papier Whatman dans l’éprouvette en vérifiant que le dépôt de pigments est bien situé au-dessus du niveau du solvant et fermer.
6. Recouvrir l’éprouvette d’un cache noir et laisser migrer le solvant à l’obscurité pendant 30 minutes.
7. Laisser sécher à l’air libre, en veillant à ce que la salle soit suffisamment aérée.
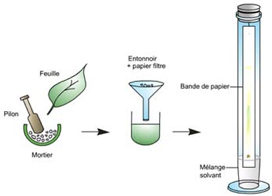 PROTOCOLE d’extraction des pigments chlorophylliens
PROTOCOLE d’extraction des pigments chlorophylliens
Découper finement 2 à 4 feuilles d’épinards, ou de plantes en ayant retiré la nervure principale, dans un mortier contenant 1 pincée de sable et 20 mL d’éthanol dénaturé.
- Broyer à l’aide du pilon jusqu’à obtention d’un liquide vert dense
- Filtrer le liquide obtenu, on récupère ainsi une solution alcoolique de pigment foliaire.
B- Comparaison du spectre d’absorption et notion de spectre d’action photosynthétique
PROTOCOLE pour le spectroscope
1. Observer dans un premier temps le spectre d’absorption en vous plaçant face à la lumière et en regardant dans l’oeilleton. Le spectre doit apparaître en entier, sinon bouger le spectroscope en direction de la lumière.
2. Mettre le pigment extrait dans le petit tube à l’aide du compte goutte.
3. Placer le tube dans le portoir (logement sur l’instrument) à l’opposé de l’oeilleton.
4. Observer à nouveau le spectre. Recommencer avec la solution alcoolique simple.
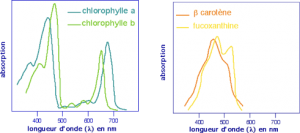
Pour que vos résultats soient les plus clairs possibles, présentez les en les associant aux courbes d’absorption suivante :