I – Campagne de vaccination
Exercice de type 2-2
Une infection par le virus H5N1, le virus de la « grippe aviaire », vient d’être diagnostiquée chez un ornithologue revenant de Thaïlande. Des confrères de l’individu malade doivent se rendre prochainement en Thaïlande pour poursuivre les recherches.
D’après l’OMS, le virus H5N1 est très pathogène et entraine la mort dans près de 60% des cas. Il se transmet lors d’un contact prolongé avec les oiseaux. Le Haut Conseil de la santé publique recommande donc la vaccination des individus exposés au virus dans le cadre de leur travail.
Vous faîtes partie du personnel du centre de vaccination de l’hôpital. Vous devez convaincre les collègues du patient atteint de se faire vacciner contre la grippe aviaire.
Document 1 : Informations de l’OMS
Les virus aviaires A(H5N1) demeurent des virus grippaux à potentiel pandémique, car ils continuent à circuler à grande échelle dans certaines populations de volailles. La plupart des personnes ne sont probablement pas immunisées contre ces virus qui peuvent occasionner chez eux de graves maladies et des décès. On ignore toutefois si le virus grippal A(H7N9) pourrait véritablement provoquer une pandémie. L’expérience a montré que certains virus grippaux de l’animal, infectant occasionnellement l’homme, n’ont pas entraîné de pandémie, alors que cela a été le cas pour d’autres. La surveillance et les investigations actuellement en cours apporteront certaines des informations nécessaires pour déterminer ce point.
D’après : http://www.who.int/mediacentre/factsheets/avian_influenza/fr/
Document 2 : Réponse primaire et réponse secondaire
Graphiques représentant les variations des concentrations en virus et l’intensité de la réponse immunitaire lors d’un premier contact avec le virus de la grippe (réponse primaire) et lors d’un deuxième contact avec le même virus (réponse secondaire)

D’après Belin TS
Document 3 : Les LT mémoires
Lors d’une réponse immunitaire une partie des lymphocytes sélectionnés se différencient en cellules effectrices, cellules qui ont une courte durée de vie (quelque jours à quelques dizaines de jours) et une autre partie se différencient en lymphocytes mémoires. De plus, certaines cellules effectrices se différencient en lymphocytes mémoires.
En comparaison avec un lymphocyte naïf (c’est-à-dire qui n’a pas rencontré d’antigène) ou effecteur, chaque lymphocyte mémoire possède une durée de vie plus longue. La longévité des cellules mémoires a pour support un clone de cellules mémoires qui se maintient au cours du temps via un processus de prolifération homéostatique : les cellules du clone se multiplient régulièrement tandis que d’autres finissent par mourir. Le pool de cellules est ainsi conservé en même temps que les propriétés de ces cellules.
Les lymphocytes mémoires ont la capacité de proliférer et de se différencier rapidement en réponse à l’antigène. Il existe aussi des plasmocytes à longue durée de vie (ou LLPC, long-lived plasma cells), qui sécrètent eux des anticorps de façon constitutive mais ne prolifèrent pas.
D’après http://acces.ens-lyon.fr
Document 4 : Composition du vaccin contre le virus H5N1
Chaque dose de 0.5 mL de vaccin a la composition suivante :
Principe actif : Antigènes purifiés du virus H5N1
3.80 µg d’hémagglutinine (protéine présente à la surface du virus)
Document 5 : Les adjuvants
Adjuvants :
• Squalène………………. 10,69 mg
• Alpha-tocopherol…… 11,86 mg
• Polysorbate 80……….. 4,86 mg
Document 5 : Les adjuvants
L’adjuvant est un produit entrant dans la composition de certains vaccins (les vaccins inactivés), afin d’augmenter l’intensité et la durée de la réponse immunitaire spécifique aux antigènes vaccinaux (au sens étymologique, adjuvant dérive du verbe latin « adjuvare » : aider).
Les adjuvants peuvent renforcer la réponse immunitaire de différentes façons dont en voici certaines :
– Ils assurent une protection aux antigènes ce qui prolonge la disponibilité de ces derniers. Ainsi l’organisme est exposé plus longtemps à l’antigène, ce qui donne davantage de temps au système immunitaire pour monter une réponse plus robuste en augmentant la production de cellules B et T nécessaires à une meilleure mémoire immunitaire pour la réponse adaptative.
– ils augmentent la réponse innée à l’antigène grâce à leur interaction avec les récepteurs PPR.
Certains vaccins sont efficaces sans adjuvants: c’est le cas notamment des vaccins à virus vivants atténués (rougeole, oreillons, rubéole, varicelle, fièvre jaune) car ces virus, une fois injectés, se multiplient rapidement dans l’organisme et leur présence suffit alors à déclencher la réaction immunitaire. C’est aussi le cas du BCG contre la tuberculose, qui est composé de bacilles vivants, là aussi atténués.
D’après http://forum-svt.ac-toulouse.fr/viewtopic.php?f=142&t=4360 Dr Brigitte Dunais
Les sels d’aluminium sont utilisés depuis les années 1950, mais une grande variété d’autres adjuvants nouveaux est en cours d’évaluation. Dans les vaccins contre la grippe pandémique A (H1N1) v, on utilise des adjuvants de type émulsions huile-dans-eau biodégradables, à base de squalène. Ils sont bien tolérés et n’induisent que des réactions locales au point d’injection ou des réactions générales (fièvre, malaise, frissons, céphalées, fatigue), toutes modérées et disparaissant après un ou deux jours, sans traitement.
D’après http://sante.lefigaro.fr/actualite/2010/03/08/10091-pourquoi-adjuvants-dans-vaccins
Pr Michèle German, immunologiste et membre de l’Académie nationale de pharmacie
Document 6 : Concentration sanguine en anticorps spécifiques du virus de la grippe aviaire après différents essais de vaccination
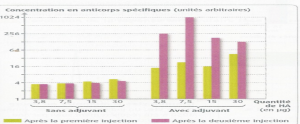
D’après Belin TS
II- Tester la présence d’antigènes
L’article L111-4 du Code de la santé publique (CSP) rend obligatoire la vaccination contre l’hépatite B pour « toute personne qui, dans un établissement public ou privé de prévention, de soins ou hébergeant des personnes âgées, exerce une activité professionnelle l’exposant à des risques de contamination ». Cet article vise aussi les étudiants et les élèves des professions de santé.
http://www.inpes.sante.fr/10000/themes/vaccination/guide-vaccination-2012/pdf/GuideVaccinations2012_Vaccination_contre_hepatite_B.pdf
Vous accueillez un nouveau membre de l’équipe dans votre service de gériatrie. Il vous présente une attestation médicale prouvant que la vaccination contre l’hépatite B a été menée à son terme mais vous devez vous assurez que les anticorps anti-HBs sont présents à une concentration supérieure à 100 mUI/ml dans son sérum. Si ce n’est pas le cas, une dose de rappel supplémentaire sera alors envisagée.
1. a. Mettre en œuvre le protocole de détection et dosage des anticorps (test de ELISA) permettant de déterminer la teneur en anticorps anti-HBs dans son sérum.
b. Pendant les temps d’attente, compléter les schémas du document 2.
2. Exploitez les résultats obtenus afin de déterminer si votre nouveau membre de l’équipe doit ou non subir un rappel supplémentaire.
Document 1 : Principe du test ELISA (Enzym Linked ImmunoSorbent Assay)
Le test Elisa est un test immunologique qui consiste à détecter et doser la présence d’un type d’anticorps dans un liquide biologique.
Pour cela, on utilise des micro puits en plastique tapissés avec l’antigène (Ag) contre lequel est dirigé l’anticorps recherché. La solution à tester est ensuite déposée dans un puits et si l’anticorps recherché (Ac1) est présent il va se lier spécifiquement à l’antigène présent au fond du puits. Un deuxième anticorps, l’anticorps traceur (Ac 2), capable de se lier à la partie constante des anticorps est alors ajouté dans le puits. Les puits sont alors vidés et rincés, ainsi les anticorps non fixés sont éliminées. L’anticorps traceur est couplé à une enzyme (E). Lorsqu’on rajoute dans le puits le substrat (S) de l’enzyme, il se forme un produit coloré. Plus le nombre d’anticorps recherché est important, plus le nombre d’anticorps traceurs fixés est important, plus la quantité de produit coloré obtenu après ajout du substrat qui est incolore est importante, plus la couleur est intense.
Document 2 : Schémas des molécules présentes en fin de test dans certains puits
Les représentations doivent rendre compte des associations moléculaires et des concentrations

Complétez le schéma du document 2 en utilisant les représentation suivante :
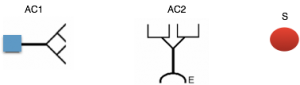
Document 3 : Matériel et PROTOCOLE ELISA
A- Matériel :
– barrette de 8 puits au fond desquels sont fixés des antigènes contre lequel est dirigé l’anticorps recherché
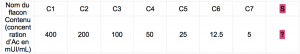
– 6 solutions d’anticorps Ac1 de concentrations différentes appelées C1, C2, C3, C4, C5, C6, C7: ces solutions ont été préparées par dilution d’une solution d’anticorps dans un tampon PBS (Phosphate buffer saline : solution saline à pH physiologique)
– solution de tampon PBS appelée C0 qui a permis les dilutions
– sérum de l’individu à tester
– solution d’un deuxième anticorps Ac2 « anti-Ac1 »: cet anticorps est associé à une enzyme peroxydase
– solution de substrat de l’enzyme peroxydase : le TMB (tétra-méthyl-benzidine)
– solution de lavage et une pipette de prélèvement
– gants, lunettes
– papier filtre, cuvette ou évier à proximité
– micropipettes et embouts jetables
– un feutre permanent, un chronomètre
– récipient avec javel pour mettre les embouts usagés
B- Protocole :
Numéroter les puits : le 1 doit être du côté de l’encoche.
- Déposer 80 µL :
- (en utilisant le même embout), de C0 dans le puits 0, C6 dans le puits 6, C5 dans le puits 5…jusqu’à C1 dans le puits 1
- après avoir changé d’embout) du sérum S de l’individu testé dans le puits S
Attention, une seule solution par puits. Les niveaux des liquides doivent être, au final, équivalents !
- Laisser incuber 10 min à température ambiante.
- Vider la barrette en la renversant horizontalement (voir schéma ci-contre) et d’un geste rapide au-dessus de l’évier (ou de la cuvette) de manière à éviter le mélange des produits.
Avant de la remettre à l’endroit, tamponner la surface des puits sur du papier filtre pour éliminer l’excès de produits et éviter la contamination.
- Remplir tous les puits avec la solution de lavage, sans débordement, et vider immédiatement comme précédemment. Répéter 2 fois ce lavage.
La solution de lavage est un tampon PBS Tween, le Tween est un détergent qui va améliorer l’efficacité du lavage.
- Mettre dans les puits 80 µL de la solution d’anticorps de détection Ac2 sur lequel est déjà fixée l’enzyme peroxydase.
Les niveaux doivent être, au final, équivalents.
- Laisser agir 10 minutes
- Vider les puits et les laver 2 fois comme au point 4.
- Mettre dans les puits 80 µL de substrat de l’enzyme peroxydase.
Les niveaux doivent être équivalents au final.
Une coloration se développe. Ne pas attendre pour comparer les colorations car au bout de quelques minutes les différences s’estompent.
III- Mieux détecter la séropositivité auVIH pour créer un test encore plus efficace
La séropositivité d’un sujet pour le VIH correspond à la présence dans son sérum d’anticorps reconnaissant certaines protéines du virus, les antigènes viraux (par exemple la protéine p24). La reconnaissance est la liaison spécifique d’un anticorps avec une région de la protéine appelée déterminant antigénique. La protéine p24 du virus comporte plusieurs déterminants antigéniques, dont l’un, appelé 5.3, est utilisé dans le test de séropositivité
Objectif : On cherche à déterminer, parmi deux anticorps, lequel est spécifique du déterminant antigénique 5.3 de la protéine p24 afin de mettre au point un test de dépistage fiable.
Matériels : ANAGENE : On dispose des fichiers anagène© de la protéine p24 et du déterminant antigénique 5.3.
RASTOP : On dispose également des fichiers rastop© de la protéine p24, de la protéine p24 associée à l’anticorps Ac1 et de la protéine p24 associée à l’anticorps Ac2
Document 1 : Structure du Virus du Sida
L’enveloppe externe
Elle est composée de lipides issus des cellules humaines et de protéines virales qui traversent cette membrane lipidique :
— La protéine gp120 qui se fixe spécifiquement sur les protéines CD4 des lymphocytes et des macrophages.
— La protéine gp 41 participe à la fusion entre l’enveloppe virale et la membrane phospholipidique de la cellule.
La capside
Elle est faite de protéines virales. Libérées après destruction du virus, elles entraînent la formation d’anticorps.
La protéine p24 est la protéine majeure de la capside. La p17 est la protéine de la matrice qui réalise la connexion entre la capside et l’enveloppe externe.
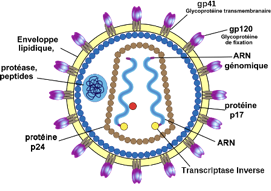
document 2: Evolution de l’infection
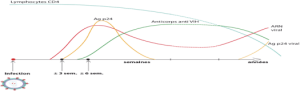
D’après http://www.afd-ld.org/~fdp_viro/content.php?page=sida
Proposer une démarche d’investigation permettant d’identifier le bon anticorps à utiliser pour mettre au point un dépistage de la séropositivité d’un patient dans les 6 semaines qui suivent une infection.
Activités et déroulement des activités :
Ouvrir dans ANAGENE le fichier « sida03.edi ». A l’aide des fonctionnalités du logiciel, mettre en évidence la région de la protéine p24 qui correspond au déterminant antigénique 5.3 ; noter, sur la fiche réponse-candidat, les numéros des acides aminés de la protéine p24 correspondant à 5.3. Appeler l’examinateur pour vérification à l’écran
Comprendre ou proposer une démarche de résolution (durée conseillée : environ 10 minutes)
Ouvrir avec le logiciel RASTOP le fichier « p24.pdb » correspondant à un modèle de la protéine. Dans la fiche réponse-candidat, expliquer l’intérêt de l’étape précédente pour retrouver le déterminant antigénique dans ce modèle de la protéine p24 (chaîne p) présent à l’écran.
Communiquer à l’aide de modes de représentation
Ouvrir les fichiers « p24_Ac1.pdb » (p24 liée à un fragment de l’anticorps Ac1) et « p24_Ac2.pdb » (p24 liée à un fragment de l’anticorps Ac2). A l’aide des fonctionnalités du logiciel RASTOP, mettre en évidence les constituants de chaque complexe moléculaire. Appeler l’examinateur pour vérification Pour les deux associations proposées « p24_Ac1.pdb » et « p24_Ac2.pdb », mettre en évidence le déterminant antigénique 5.3 à l’aide des fonctionnalités du logiciel RASTOP. Appeler l’examinateur pour vérification (écran à organiser)
Communiquer à l’aide de modes de représentation
Présenter des images des modèles moléculaires traités précédemment de manière judicieuse pour répondre au problème posé (penser à modifier judicieusement la couleur du fond pour la lisibilité à l’impression), soit numériquement (capture d’image utilisée dans un traitement de texte, ou autre logiciel), soit à la main après impression des images. Enregistrer à votre nom, à l’emplacement qui vous est indiqué.
Appliquer une démarche explicative
Déduire des résultats obtenus sur la fiche réponse-candidat, quel est l’anticorps spécifique du déterminant antigénique 5.3 de la protéine p24
